中国网财经9月6日讯 昨日,全球首款FcRn拮抗剂艾加莫德(卫伟迦)正式在国内上市,北京、上海、广东、湖北、河南、江西、河北等全国多个省市开出首批处方。
今年6月,卫伟迦(艾加莫德α注射液)获国家药监局批准上市,与常规治疗药物联合,用于治疗乙酰胆碱受体(AChR)抗体阳性的成人全身型重症肌无力患者。从国内获批到正式惠及患者仅用时67天,创下了国内进口生物制剂从获批到上市的最快记录。
艾加莫德在国内的获批是基于已发表在国际权威学术期刊《柳叶刀•神经病学》的全球3期多中心临床研究ADAPT的结果。再鼎医药医学事务部执行总监李想表示,临床研究中,艾加莫德已经证实了其能够帮助患者改善肌肉力量和生活质量,在第一个治疗周期中MG-ADL改善≥2分的患者高达77.8%,QMG改善≥3分的患者高达74.2%,40%的患者在第一个周期即达到最小临床表现,有望帮助患者实现“双达标”的理想治疗状态,为全身型重症肌无力患者实现“疾病缓解+生活质量提高”带来了新可能,有望达到“带病但不发病”的正常生活状态。
资料显示,重症肌无力(MG)是一种慢性、自身免疫性神经肌肉疾病,由神经-肌肉接头传递功能障碍引起,其特征是肌肉无力的反复发生和易疲劳,我国年发病率为0.68/10万。国外数据显示,超过85%的MG患者在发病18个月内进展为全身型重症肌无力(gMG)。早在2018年,全身型重症肌无力即已被纳入国家五部委联合发布的《第一批罕见病目录》。
同日,由中国初级卫生保健基金会发起、再鼎医药公益支持的国内首个全身型重症肌无力患者关爱平台——“重症肌无力加油站”正式启动上线。这也是国内首个MG患者全病程管理平台,旨在为长期以来饱受疾病困扰的gMG患者赋能助力,帮助MG患者回归正常生活和工作。
再鼎医药首席商务官、大中华区总裁梁怡表示,艾加莫德是再鼎布局自身免疫领域的第一款产品,目前正在其他多项自身免疫性疾病中开展临床研究。

 6年来首次更新!特斯拉发布
6年来首次更新!特斯拉发布
 美军集束炸弹袭击幸存者:家
美军集束炸弹袭击幸存者:家
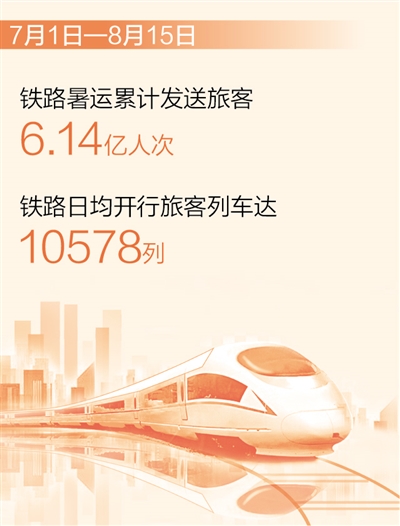 铁路暑运累计发送旅客超6亿
铁路暑运累计发送旅客超6亿
 警惕大股东质押式减持
警惕大股东质押式减持
 半导体板块涨3.46% 利扬芯
半导体板块涨3.46% 利扬芯
 深圳前海综保区9月进出口创
深圳前海综保区9月进出口创
 作业帮与利亚德签订战略合作
作业帮与利亚德签订战略合作
 深圳坪山新能源车产业园一期
深圳坪山新能源车产业园一期

 48小时点击排行
48小时点击排行


